| Pate Minh Chay chứa độc tố có thể gây tử vong Bộ Y tế: Hạn chế tới mức thấp nhất các trường hợp tử vong do bệnh bạch hầu Khuyến cáo: Ăn sắn luộc không đúng cách, 1 cháu bé bị ngộ độc tử vong |
Cục Quản lý Dược – Bộ Y tế vừa có công văn về việc về việc dừng sử dụng Dung dịch thuốc tiêm Bupivacaine WPW Spinal 0,5% Heavy có SĐK: VN-20879-17. Thuốc do Công ty Warsaw Pharmaceutical Work Polfa S.A (Poland) sản xuất, Công ty cổ phần dược phẩm Trung ương CPC1 nhập khẩu.
Cụ thể, ngày 22/10/2020, Cục Quản lý Dược nhận được các công văn: Công văn số 2491/SYT-NVD ngày 22/10/2020 của Sở Y tế tỉnh Bình Dương báo cáo các ca nghi ngộ độc sử dụng bupivacain cho gây tê tủy sống và Công văn số 140/TTT ngày 22/10/2020 của Trung tâm DI & ADR quốc gia về việc cung cấp thông tin các báo cáo phản ứng có hại của thuốc liên quan đến Dung dịch thuốc tiêm Bupivacaine WPW Spinal 0,5% Heavy (Bupivacain hydroclorid 5mg/ml), SĐK: VN-20879-17, các lô: 04DB1119, lô 07DB0919 và lô 08DB0919.
Theo các công văn, có 03/04 ca ADR nghiêm trọng (tử vong) sau khi dùng thuốc trên để gây tê tủy sống.
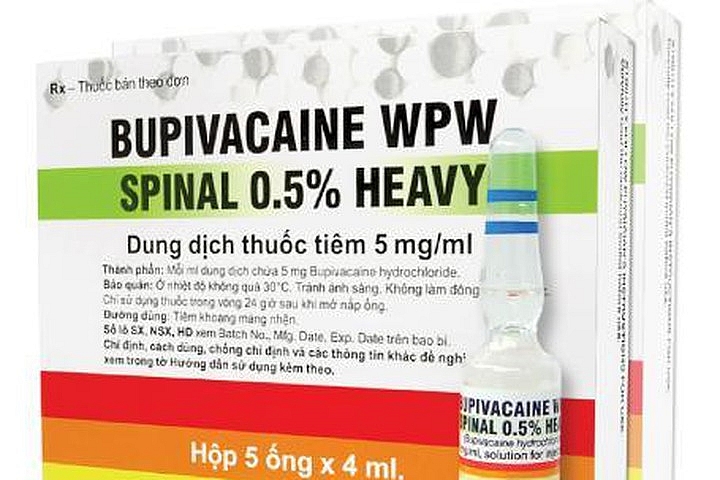 |
| Nghi vấn tử vong sau khi dùng thuốc do Dược phẩm Trung ương CPC1 nhập khẩu |
Cục Quản lý Dược đã đề nghị các Sở Y tế, các bệnh viện trực thuộc Bộ Y tế trong thời gian chờ xác định nguyên nhân tai biến, khẩn trương chỉ đạo các cơ sở khám chữa bệnh không tiếp tục sử dụng thuốc Dung dịch thuốc tiêm Bupivacaine WPW Spinal 0,5% Heavy, SĐK: VN-20879-17, các lô: 04DB1119, 07DB0919 và lô 08DB0919.
Cùng với đó, chỉ đạo các cơ sở sử dụng trên địa bàn đảm bảo cung ứng và tìm nguồn thay thế trong trường hợp cần thiết đối với thuốc tiêm chứa Bupivacain; tăng cường công tác dự phòng, phát hiện và xử lý tai biến có thể xảy ra trong quá trình sử dụng dung dịch thuốc tiêm Bupivacaine WPW Spinal 0,5% Heavy, SĐK: VN-20879-17.
Cục Quản lý Dược yêu cầu Công ty cổ phần dược phẩm Trung ương CPC1 rà soát tình hình phân phối, sử dụng Dung dịch thuốc tiêm Bupivacaine WPW Spinal 0,5% Heavy, SĐK: VN-20879-17, số lô: 07DB0919, 08DB0919 và 04DB1119, thông báo đến các đơn vị liên quan không tiếp tục phân phối, sử dụng các lô thuốc trên cho đến khi có ý kiến kết luận cuối cùng của các cơ quan chức năng liên quan.
Được biết, đầu tháng 1/2020, Cục Quản lý Dược có Công văn số 232/QLD-CL về việc xử lý Dung dịch thuốc tiêm Bupivacaine 5mg/ml, SĐK: VN-20879-17. Theo đó, các lô thuốc tiêm Bupivacaine WPW Spinal 0,5% Heavy, SĐK: VN- 20879-17, Số lô: 03DB0319, 05DB0319, 01DB0619, 03DB0919, 04DB0919 và 05DB0919 do Công ty Warsaw Pharmaceutical Work Polfa S.A., Poland (Ba Lan) sản xuất, đạt tiêu chuẩn chất lượng và được phép sử dụng.
 |
| Công ty Dược phẩm Trung ương CPC1 |
Thế nhưng chỉ 5 tháng sau (tháng 6/2020), Sở Y tế Quảng Bình nhận được Báo cáo số 312/BC-BV ngày 08/6/2020 của Bệnh viện Đa khoa Khu vực Bắc Quảng Bình về việc Báo cáo nhanh trường hợp tử vong liên quan người bệnh được gây tê tủy sống (chẩn đoán chỉ định: Nội soi niệu quản ngược dòng tán sỏi bằng Laser) bằng thuốc Bupivacaine WPW Spinal 0,5% Heavy (SĐK: VN-20879-17; số lô: 04DB0919; ngày sản xuất: 11/9/2019; hạn sử dụng: 11/9/2021; nước sản xuất: Ba Lan). Sau khi gây tê khoảng 10 phút, bệnh nhân đột ngột ngừng tuần hoàn, hô hấp. Bệnh viện Đa khoa Khu vực Bắc Quảng Bình đã niêm phong lô thuốc Bupivacaine WPW Spinal 0,5% Heavy đã sử dụng ở trên để xác định nguyên nhân.
Tính tới tháng 11/2019, tại Đà Nẵng đã có hai sản phụ tử vong, một nguy kịch sau khi mổ lấy thai, nghi do thuốc gây tê Bupivacaine WPW Spinal 0,5 Heavy. Cùng với đó các tỉnh thành Hà Nội, Quảng Ngãi, Bến Tre, Long An, Cần Thơ cũng đồng loạt lên tiếng sau khi bệnh nhân bị tụt huyết áp kéo dài, giãn cơ, rơi vào nguy hiểm khi sử dụng thuốc tiêm trên.
| Công ty Cổ phần Dược phẩm trung ương CPC1 được hình thành từ năm 1945 ngay sau khi hòa bình lập lại trên miền Bắc. Do quy mô và phạm vi hoạt động còn nhỏ hẹp nên ban đầu còn là một đơn vị trực thuộc Bộ Nội thương với tên gọi là Công ty thuốc Nam – thuốc Bắc. Đến năm 1956 Công ty chuyển về Bộ Y tế quản lý, trực thuộc Cục phân phối Dược phẩm với tên “Quốc doanh Y Dược phẩm Trung ương”. Công ty chính thức được thành lập theo quyết định số 171/BYT-QĐ ngày 1/4/1971 với tên gọi “Công ty Dược phẩm cấp I” thuộc Tổng Công ty Dược (Bộ Y tế). Năm 1985, Công ty đổi tên thành “Công ty Dược phẩm Trung ương I” theo quyết định số 534/BYT-QĐ ngày 5/6/1985. Ngày 22/4/1993, Bộ Y tế ra Quyết định số 408/BYT - QĐ thành lập lại “Công ty Dược phẩm Trung ương 1” thuộc Tổng Công ty Dược, Bộ Y tế. Đến năm 2010, Công ty chuyển đổi thành Công ty TNHH Một thành viên Dược phẩm trung ương 1 theo quyết định số 45/QĐ-TCTD ngày 29/6/2010 do Nhà nước làm chủ sở hữu. Năm 2016, Công ty chuyển đổi thành Công ty Cổ phần Dược phẩm trung ương CPC1 - tên hiện nay theo quyết định số 2290/QĐ-BYT ngày 12/06/2015 của Bộ Y Tế. |














































































