 |
| Dược liệu Đan sâm bị yêu cầu thu hồi do không đạt chất lượng (ảnh minh họa) |
Cục Quản lý Y, Dược cổ truyền vừa qua ban hành Công văn số 685/YDCT-QLD ngày 5/7/2021 về việc xử lý lô dược liệu Đan sâm (số lô NK/DS.110220, NSX: 11/02/2020, hạn dùng 24 tháng từ NSX) không đạt chất lượng do Công ty Cổ phần Xuất nhập khẩu Dược liệu Dương Thư (nay đổi tên là Công ty Cổ phần dược liệu Quốc tế) sản xuất.
Cũng trong thời gian này, Cục quản lý Y, Dược cổ truyền chỉ đạo các doanh nghiệp thu hồi toàn bộ sản phẩm dược liệu Đan sâm được phân phối tại Công ty TNHH Đông dược Phúc Hưng (địa chỉ tại 98 Nguyễn Viết Xuân, phường Quang Trung, quận Hà Đông, TP Hà Nội), Công ty TNHH Thiên Ân Dược (Lô BT 34 - 39, Khu dân cư Dịch vụ Đấu giá và tạo vốn xây dựng cơ sở hạ tầng, phường Đình Bảng, thị xã Từ Sơn, tỉnh Bắc Ninh) và Công ty CP Dược phẩm Hà Tây (số 10A phố Quang Trung, Phường Quang Trung, Quận Hà Đông, TP. Hà Nội).
 |
| Công văn số 685/YDCT-QLD ngày 5/7/2021 về việc xử lý lô dược liệu Đan sâm |
Cụ thể, thu hồi lô dược liệu Đan sâm tại Công ty CP Dược phẩm Hà Tây có số lô: 708092020, NSX: 07/09/2020, hạn dùng: 03/2022. Sản phẩm được phân phối tại Công ty TNHH Đông dược Phúc Hưng và Công ty TNHH Thiên Ân Dược có số lô: YL-DS-190902, NXS: 22/08/2019, hạn dùng: 21/08/2021. Theo đó, dựa trên kết quả báo cáo của Viện Kiểm nghiệm thuốc Trung ương đối với dược liệu Đan sâm lấy tại Bệnh viện Đa khoa Đức Giang, số sản phẩm này không đạt chỉ tiêu về định lượng Tanshinon IIA có trong thành phần.
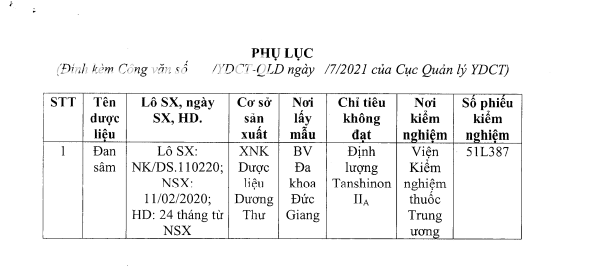 |
| Phụ lục đính kèm số 685/YDCT-QLD ngày 5/7/2021 về việc xử lý lô dược liệu Đan sâm |
Hồ sơ thu hồi bao gồm thông tin nguồn gốc xuất xứ, số lượng phân phối, ngày sản xuất, báo cáo trúng thầu số lượng thu hồi, các bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua dược liệu .
Đồng thời, các công ty phân phối dược liệu Đan sâm phối hợp với Cơ quan kiểm tra chất lượng, cơ quan kiểm nghiệm thuốc Nhà nước tiến hành lấy 01 mẫu bổ sung và gửi mẫu đã lấy tới Viện kiểm nghiệm thuốc Trung ương để kiểm tra chất lượng đối với chỉ tiêu định lượng Tanshinon IIA .
Liên quan đến nội dung này, Sở Y tế Hà Nội phát hành Công văn số 10449/SYT-NVD ngày 9/7/2021 gửi đến thủ trưởng các cơ sở y tế trên địa bàn, phòng Y tế các quận, huyện, thị xã về việc dược liệu Đan sâm không đạt tiêu chuẩn chất lượng chỉ tiêu Định lượng Tanshinon IIA của các lô dược liệu Đan sâm được phân phối tại các doanh nghiệp sản xuất, kinh doanh.
Sở Y tế Hà Nội yêu cầu các cơ sở y tế công lập trực thuộc ngành, các cơ sở y tế ngoài công 1 các cơ sở kinh doanh dược liệu trên địa bàn khẩn trương rà soát, thu hồi các dược liệu Đan sâm không đạt tiêu chuẩn chất lượng. Bên cạnh đó, phòng Y tế các quận, huyện, thị xã phải thông báo đến các cơ sở hành nghề trên địa bàn quản lý; tiến hành kiểm tra, giám sát việc thực hiện thu hồi sản phẩm.
 |
| Công văn số 10449/SYT-NVD ngày 9/7/2021 của Sở Y tế Hà Nội |
Liên quan tới vấn đề quản lý chất lượng dược liệu, vị thuốc cổ truyền, trước đó, Bộ Y tế cũng đưa ra lấy ý kiến nhân dân về dự thảo Thông tư quy định về chất lượng dược liệu, thuốc cổ truyền. Theo đó, Bộ đề xuất quy định quản lý chất lượng dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trong quá trình kinh doanh, lưu hành và sử dụng.
Cụ thể, Bộ Y tế đề xuất yêu cầu quản lý chất lượng dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trong quá trình kinh doanh: Áp dụng nguyên tắc, tiêu chuẩn thực hành tốt trong suốt quá trình kinh doanh, phù hợp với phạm vi kinh doanh của cơ sở. Đối với cơ sở chuyên bán lẻ dược liệu, vị thuốc cổ truyền, thuốc cổ truyền phải áp dụng các điều kiện bán lẻ dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trong suốt quá trình kinh doanh theo quy định hiện hành.
Dược liệu, nguyên liệu sản xuất thuốc cổ truyền, bao bì tiếp xúc trực tiếp với thuốc cổ truyền trước khi đưa vào sản xuất thuốc cổ truyền phải được cơ sở sản xuất tiến hành kiểm nghiệm và đạt tiêu chuẩn chất lượng. Dược liệu, vị thuốc cổ truyền, thuốc cổ truyền trước khi xuất xưởng phải được cơ sở sản xuất tiến hành kiểm nghiệm và đạt tiêu chuẩn chất lượng.
Người đứng đầu và người phụ trách chuyên môn của cơ sở kinh doanh; người phụ trách về bảo đảm chất lượng của cơ sở sản xuất phải chịu trách nhiệm về công tác quản lý chất lượng và kiểm tra chất lượng dược liệu, thuốc cổ truyền tại cơ sở.













































































