Cảnh báo thuốc Cefuroxim 500 giả đang lưu hành trên thị trường
Cục Quản lý Dược (Bộ Y tế) yêu cầu Sở Y tế các tỉnh thành phối hợp với các cơ quan truyền thông, thông tin tới các cơ sở buôn bán, sử dụng thuốc và người dân biết để không buôn bán, sử dụng sản phẩm CEFUROXIM 500 giả.
| Bộ Y tế cảnh báo thuốc Nexium lưu hành trái phép Cảnh báo thuốc Salonpas Gel nghi giả rao bán trên các trang mạng xã hội |
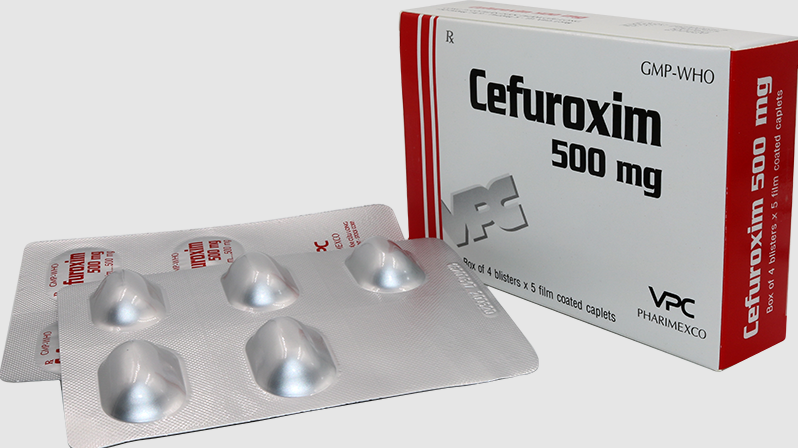 |
| Thuốc Cefuroxim 500 |
Theo đó, Cục Quản lý Dược nhận được Công văn của Trung tâm Kiểm nghiệm thuốc, mỹ phẩm, thực phẩm Hà Nội kèm phiếu kiểm nghiệm số 2127/KNT-22 báo cáo về mẫu sản phẩm trên nhãn ghi: Viên nén dài bao phim CEFUROXIM 500, SĐK: VD-27836-17, lô SX: 71240820, NSX: 240820, HD: 240823.
Mẫu do Trung tâm kiểm nghiệm thuốc, mỹ phẩm, thực phẩm Hà Nội lấy tại Công ty TNHH Dược phẩm Đa Phúc - Thôn 5, xã Phú Cát, huyện Quốc Oai, Hà Nội.
Kết quả cho thấy, mẫu sản phẩm trên có hình thức nhãn và hình thức viên không giống mẫu thuốc thật, không có phản ứng định tính Cefuroxim. Tuy nhiên sản phẩm này lại có phản ứng định tính với Paracetamol, hàm lượng Paracetamol là 319,2 mg/viên.
Sau khi đối chiếu, xem xét, để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thông tin về thuốc giả trên nhãn ghi: Viên nén dài bao phim CEFUROXIM 500, SĐK: VD-27836- 17, lô SX: 71240820, NSX: 240820, HD: 240823.
 |
| Dấu hiệu phân biệt thuốc giả và thuốc thật. |
Đồng thời, Cục Quản lý Dược đã chỉ ra đặc điểm, dấu hiệu phân biệt thuốc giả với thuốc thật như sau: Chữ in trên nhãn hộp thuốc giả có phông chữ sai khác so với thuốc thật.
Ngoài ra, một số chữ trên bao bì thuốc giả bị lệch so với bao bì thuốc thật. Xung quanh viền thuốc giả in số lô - hạn sử dụng trên vỉ có sai khác so với thuốc thật. Thuốc giả có viền xung quanh nhẵn bóng, thuốc thật có viền xung quanh có gai.
Viên thuốc thật là viên nén dài, bao phim màu trắng, mặt và cạnh trơn bóng. Thuốc giả cũng là viên nén dài màu trắng nhưng không trơn bóng, thành cạnh không sắc nét.
 |
Cục Quản lý Dược đã yêu cầu Sở Y tế các tỉnh thành phối hợp với các cơ quan truyền thông, thông tin tới các cơ sở buôn bán, sử dụng thuốc và người dân biết để không buôn bán, sử dụng sản phẩm CEFUROXIM 500 giả có các dấu hiệu nhận biết nêu trên.
Phối hợp với các cơ quan chức năng liên quan tiến hành kiểm tra các cơ sở kinh doanh thuốc trên địa bàn; xác minh thông tin và truy tìm nguồn gốc về sản phẩm CEFUROXIM 500 giả nêu trên, xử lý các tổ chức, cá nhân vi phạm theo quy định hiện hành; kịp thời phát hiện và ngăn chặn việc sản xuất, buôn bán và sử dụng thuốc CEFUROXIM 500 giả. Báo cáo kết quả kiểm tra, xử lý vi phạm và nguồn gốc lô thuốc giả về Cục Quản lý Dược.
Thuốc CEFUROXIM 500 thuộc nhóm kháng sinh, được chỉ định điều trị nhiễm khuẩn do vi khuẩn nhạy cảm gây ra: Đường hô hấp dưới: Viêm phổi, viêm phế quản cấp và mạn; Đường hô hấp trên: Viêm tai giữa, viêm xoang, viêm amiđan, viêm họng; Đường niệu – sinh dục: Viêm bể thận, viêm bàng quang, viêm niệu đạo; Da và mô mềm: mủ nhọt, chốc lở. Điều trị bệnh Lyme thời kỳ đầu biểu hiện bằng chứng ban đỏ da loang do Borrelia burgdorferi…. Cefuroxim 500 là thuốc kê đơn, người bệnh không tự ý sử dụng khi chưa có chỉ định của bác sĩ.
|
Theo Nghị định số 185/2013/NĐ-CP ngày 15/11/2013 của Chính phủ quy định xử phạt vi phạm hành chính trong hoạt động thương mại, sản xuất, buôn bán hàng giả, hàng cấm và bảo vệ quyền lợi người tiêu dùng và Nghị định số 124/2015/NĐ-CP ngày 19/11/2015 về sửa đổi, bổ sung một số điều của Nghị định số 185/2013/NĐ-CP, kinh doanh hàng hóa không rõ nguồn gốc, xuất xứ có thể bị phạt tiền từ 30 - 40 triệu đồng. Tại Nghị định số 117/2020/NĐ-CP ngày 28/9/2020 của Chính phủ quy định xử phạt vi phạm hành chính trong lĩnh vực y tế, hành vi sản xuất, kinh doanh thuốc chữa bệnh chưa được phép lưu hành hoặc mới thử nghiệm, chưa được phép sản xuất, nhập khẩu có thể bị phạt tiền từ 60 - 80 triệu đồng. Ngoài ra, trường hợp gây chết người hoặc tổn hại nghiêm trọng đến sức khỏe người khác, người vi phạm có thể bị xử lý hình sự. |